나노 로봇이 혈액을 타고 인체에 들어가 암세포를 공격하는 모습을 상상한 그림
한편으로는 의학 발전이 끊임없이 이뤄지고 있는데도 암을 극복할 수 있는 속시원한 치료법이 아직까지 개발되지 않아 암 환자의 운명을 조기진단과 치료에 맡겨야 하는 실정이다. 나이가 들수록 암 발병률이 높아지는 이유는 과연 무엇일까. 인류 최대의 질병 가운데 하나로 손꼽히는 암은 우리 몸을 구성하는 정상 세포가 유전적 결함이나 돌연변이 등으로 인해 비정상적이고 무질서한 성장과 증식을 계속하는 현상이다. 대부분의 암은 1개의 이상한 세포(암 세포)가 증식해서 발생하는데, 이들이 다른 조직에 침입해 정상적인 작용을 방해하면서 해당 개체를 죽음에 이르게 한다.
일반적으로 암은 40대 이후에 발생하기 시작하며, 나이가 들수록 발병률이 계속 높아진다. 하지만 이런 현상은 ‘세포분열을 억제하면 암도 억제된다’는 기존의 과학적 상식에 비춰봤을 때 매우 역설적이다. 노화가 진행되면 세포분열 능력도 떨어져 암 세포의 증식도 당연히 억제돼야 하기 때문이다. 세포분열 능력이 현저하게 떨어진 노화세포가 어떻게 활발하게 분열하면서 암세포로의 성장과 증식을 계속하는지는 오랜 기간 풀리지 않는 수수께끼였다.
그런데 이 수수께끼를 푸는 열쇠가 될 수 있는 연구 결과가 2004년 12월26일, 국내 연구진에 의해 발표됐다. 조선대 의과대학 유호진 교수(43·약리학) 연구팀은 노화가 진행되면서 세포분열 능력이 떨어지면 유전자 복구 시스템의 기능도 함께 망가져 돌연변이를 증가시키고 결국 암 발병을 촉진하게 된다는 사실을 세계 최초로 규명했다고 밝혔다. 유 교수 연구팀은 세포자살과 세포분열을 동시에 억제하는 기능을 갖고 있는 ‘Bcl-2’라는 단백질에 주목했다.
세포자살, 분열 동시 억제 ‘Bcl-2’ 단백질
우리 몸은 60조~100조 개의 세포로 구성돼 있는데, 이 세포들은 생로병사의 과정을 거치면서 자연스럽게 소멸한다. 즉 몸은 세포들이 적시적소에서 분열하고 소멸해야 생명을 유지할 수 있다. 정상 세포는 흡연이나 자외선, 스트레스 등 외부의 유해인자가 침입해올 경우 여러 가지 방어체계를 작동하면서 세포의 손상을 최소화한다. 설사 외부의 유해인자에 의해 세포가 손상된다 하더라도 세포에 존재하는 복잡하고 정교한 유전자 복구 시스템이 작동해 쉽게 복구되기 때문에 암으로 발전하지 않는다. 과도한 유전자 손상이 일어날 경우, 세포 자살프로그램이 작동하면서 돌연변이를 제거해 암 발병을 막아주기 때문이다.
자살프로그램이란 유전자에 제어되는 능동적인 세포의 죽음을 의미한다. 세포의 자살프로그램은 개체의 탄생 과정에서 형태를 만들고, 성체에서는 정상 세포를 갱신하거나 암 등 비정상적인 세포를 제거하는 일을 담당한다.
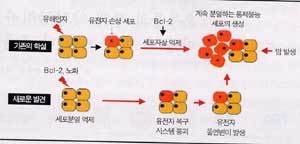
유호진 교수가 밝혀낸 노화와 암 발생 간의 상관관계.
“세포분열 억제로 암 억제” 기존 학설 뒤집어
유전자 복구 시스템과 자살프로그램은 서로 협동하면서 우리 신체의 건강과 균형을 유지하게끔 도와준다. 예를 들어 유전자가 손상되면 1차적으로 유전자 복구 시스템이 작동하면서 원래의 상태로 되돌린다. 하지만 유전자의 손상 정도가 커 복구할 수 있는 범위를 넘어서면 돌연변이가 이뤄지는데, 그 순간 돌연변이는 자살프로그램에 의해 파괴된다. 따라서 유전자 복구 시스템이나 자살프로그램이 제때에 작동하지 않으면 돌연변이 증가로 인해 암이 발병하는 것이다.
최근까지의 학설에 따르면 암 발병과 암 세포 증식은 세포의 자살프로그램이 원활하게 작동하지 않을 경우 생기며, 세포분열을 억제하면 암이 억제된다는 것이었다. 따라서 암과 관련된 수많은 연구의 방향도 이 부분에 초점이 맞춰져 있었다.
하지만 이번 연구 결과는 세포분열을 억제하면 유전자 복구 시스템도 함께 망가져 돌연변이가 기하급수적으로 늘어나면서 오히려 암 발병이 촉진된다는 새로운 사실을 밝혀냈다는 점에서 큰 의미가 있다. 연구팀은 세포자살과 세포분열 억제라는 두 가지 기능을 가진 Bcl-2 단백질을 세포분열 억제 기능만 갖게 변형시킨 뒤 세포에 투입한 결과, 마찬가지로 암이 발병한다는 사실을 확인했다고 밝혔다. 즉 Bcl-2 단백질에 의해 세포분열이 억제되거나 나이가 들어 세포분열 능력이 떨어지면 유전자 복구 시스템의 기능이 망가지고, 그 결과 세포 내 유전자에 손상물들이 축적돼 돌연변이가 발생하면서 결국 통제할 수 없는 세포분열로 이어져 암 발병이 촉진될 수 있다는 것이다.

조선대 유호진 교수
서울대 생명과학부 학부장 정진하 교수는 “이번 연구 결과는 노화 세포에서 왜 암 발생이 빈번하게 일어나는지를 설명할 수 있는 이론적 근거가 됐다”면서 “노화와 암 발생의 연관성 연구에 새로운 전기가 마련될 것”이라고 평가했다. 국내 연구진에 의해 밝혀진 새로운 연구 결과에 따라 유전자 복구 시스템의 붕괴 억제제가 성공적으로 개발된다면 나이가 들어도 암에 대한 공포에서 한 발짝 비켜날 수 있을 전망이다.
















